Tiêu chuẩn GMP được biết đến là một trong những yêu cầu bắt buộc trong ngành Dược. Vậy trên thực tế, GMP là gì và đâu là những điều mà bạn cần nhớ để đảm bảo tiêu chuẩn GMP? Hãy cùng Sapo.vn tìm hiểu ngay trong những chia sẻ dưới đây.
1. Tiêu chuẩn GMP là gì?
Tiêu chuẩn GMP (Good Manufacturing Practices) là bộ nguyên tắc và hướng dẫn về thực hành sản xuất tốt, nhằm đảm bảo sản phẩm được sản xuất và kiểm soát đồng nhất về chất lượng, an toàn và đáp ứng yêu cầu của cơ quan quản lý. GMP quy định các tiêu chí trong toàn bộ quá trình sản xuất như nhà xưởng, thiết bị, nguyên liệu, quy trình sản xuất, vệ sinh, kiểm soát chất lượng và đào tạo nhân sự.

Tiêu chuẩn này được áp dụng phổ biến trong các ngành dược phẩm, thực phẩm, mỹ phẩm, thực phẩm chức năng và thiết bị y tế, giúp doanh nghiệp giảm rủi ro sai lỗi trong sản xuất và đảm bảo sản phẩm đạt chuẩn trước khi đưa ra thị trường.
Tầm quan trọng của tiêu chuẩn GMP nằm ở việc giúp doanh nghiệp:
- Đảm bảo chất lượng và độ an toàn của sản phẩm trước khi đưa ra thị trường.
- Giảm thiểu rủi ro trong quá trình sản xuất như nhiễm chéo, sai quy trình hoặc lỗi kiểm soát chất lượng.
- Đáp ứng yêu cầu pháp lý của cơ quan quản lý, đặc biệt trong các ngành có yêu cầu kiểm soát nghiêm ngặt như dược và thực phẩm.
- Nâng cao uy tín và khả năng cạnh tranh của doanh nghiệp, tạo niềm tin cho người tiêu dùng và đối tác.
2. Đặc điểm cốt lõi quan trọng của GMP
Tiêu chuẩn GMP tập trung vào việc kiểm soát toàn bộ quá trình sản xuất nhằm đảm bảo sản phẩm luôn đạt chất lượng ổn định và an toàn. Một số đặc điểm cốt lõi của GMP bao gồm:

- Kiểm soát chặt chẽ quy trình sản xuất: Mọi công đoạn từ tiếp nhận nguyên liệu, sản xuất, đóng gói đến bảo quản đều phải được xây dựng quy trình rõ ràng và thực hiện theo tiêu chuẩn thống nhất để hạn chế sai sót.
- Đảm bảo điều kiện nhà xưởng và thiết bị: Nhà xưởng phải được thiết kế phù hợp với quy trình sản xuất, đảm bảo vệ sinh, hạn chế nhiễm chéo. Thiết bị sản xuất cần được bảo trì, hiệu chuẩn và vệ sinh định kỳ.
- Kiểm soát chất lượng nguyên liệu và sản phẩm: Nguyên liệu đầu vào, bán thành phẩm và thành phẩm đều phải được kiểm tra và ghi nhận đầy đủ, giúp đảm bảo sản phẩm cuối cùng đáp ứng tiêu chuẩn chất lượng.
- Quản lý hồ sơ và truy xuất nguồn gốc: Tất cả hoạt động sản xuất cần được ghi chép, lưu trữ hồ sơ đầy đủ, giúp doanh nghiệp có thể truy xuất nguồn gốc và kiểm tra lại khi cần thiết.
- Đào tạo và quản lý nhân sự: Nhân sự tham gia sản xuất phải được đào tạo về quy trình, vệ sinh và an toàn sản xuất, đồng thời tuân thủ các quy định nghiêm ngặt trong môi trường sản xuất GMP.
3. Các loại GMP phổ biến
Tiêu chuẩn GMP trong ngành Dược uy tín và đáng tin cậy trên thế giới bao gồm: Tiêu chuẩn EU GMP, tiêu chuẩn GMP WHO, tiêu chuẩn cGMP,...
- Tiêu chuẩn EU GMP: là tiêu chuẩn thực hành sản xuất tốt EU được cấp bởi EMA - cơ quan quản lý Dược châu Âu. Đây được xem là một trong các loại tiêu chuẩn GMP chịu trách nhiệm trong việc đánh giá khoa học, kiểm tra cũng như giám sát an toàn các loại thuốc trong EU. EU GMP được xem là một trong những chuẩn mực có chất lượng cao nhất.
- Tiêu chuẩn GMP WHO: Đây là hướng dẫn thực hành tốt sản xuất thuốc do tổ chức y tế thế giới xây dựng và được phát hành đầu tiên vào năm 1968. Tiêu chuẩn này được hầu hết các cơ sở sản xuất thuốc ở Việt Nam áp dụng và thực hiện theo.
- Tiêu chuẩn cGMP: Tiêu chuẩn này được áp dụng trong các nhà máy, xưởng và cơ sở sản xuất,...nhằm đảm bảo tuyệt đối chất lượng và tính an toàn cho sản phẩm.
4. Yêu cầu về tiêu chuẩn GMP
Đối với các tiêu chuẩn GMP trong ngành dược, doanh nghiệp sản xuất cần thực hiện và đảm bảo các yêu cầu sau:

- Yêu cầu nhân sự: Nhân sự cần được sắp xếp và đánh giá phù với năng lực, trình độ. Cùng với đó là xây dựng các quy định nghiêm ngặt về quy trình kiểm tra sức khỏe gồm các hạng mục như trí lực, thể lực, bệnh tật của nhân sự, đặc biệt là các công nhân sản xuất trực tiếp.
- Yêu cầu về thiết kế, xây dựng, lắp đặt nhà xưởng và máy móc, thiết bị chế biến: Doanh nghiệp sản xuất cần quy định rõ ràng về vị trí xây dựng nhà máy, vị trí lắp đặt thiết bị để đảm bảo hiệu quả tạo ra các sản phẩm chất lượng, an toàn.
- Yêu cầu kiểm soát vệ sinh nhà xưởng, môi trường: Nguồn nước đầu vào, xử lý nước thải đầu ra, sản phẩm phụ, rác thải để đảm bảo vệ sinh môi trường và nhà xưởng là yếu tố đặc biệt quan trọng mà doanh nghiệp cần chú trọng. Đây là tiêu chuẩn GMP bắt buộc để doanh nghiệp có thể sản xuất dược phẩm đảm bảo vệ sinh và chất lượng.
- Yêu cầu về kiểm soát quá trình chế biến: Các doanh nghiệp cần thực hiện nghiêm túc việc xây dựng quy định về phương pháp chế biến cũng như thủ tục, hướng dẫn công việc cụ thể và đảm bảo các tiêu chuẩn về nguyên liệu, công thức pha chế. Đặc biệt, doanh nghiệp cũng cần các biện pháp giám sát và kiểm tra trong quá trình sản xuất thuốc.
- Yêu cầu về kiểm soát quá trình bảo quản và phân phối sản phẩm: Các doanh nghiệp sản xuất thuốc, dược phẩm cần đưa ra yêu cầu về việc bảo quản, vận chuyển sao cho thành phẩm không bị nhiễm bẩn hay bị tác động bởi các tác nhân hóa học, vật lý, vi sinh và không thay đổi chất lượng.
Xem thêm: GSP là gì? Cách xây dựng kho thuốc theo tiêu chuẩn GSP
5. Quy trình chứng nhận GMP
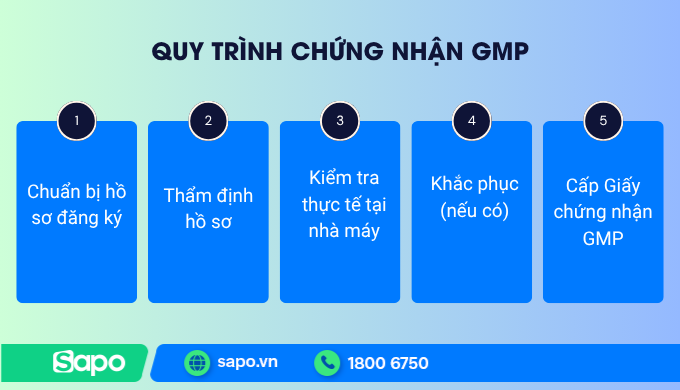
Bước 1: Cơ sở sản xuất gửi hồ sơ đăng ký kiểm tra GMP gửi về Cục Quản lý Dược Bộ Y tế
Bước 2: Cục quản lý Dược tiếp nhận, kiểm tra và thẩm định hồ sơ. Nếu hồ sơ chưa đáp ứng yêu cầu, Cục sẽ có văn bản yêu cầu cơ sở bổ sung.
Bước 3: Trong thời gian 60 ngày kể từ ngày nhận hồ sơ hợp lệ, Cục quản lý Dược có quyết định thành lập đoàn kiểm tra các hoạt động của cơ sở sản xuất theo các nguyên tắc tiêu chuẩn GMP-WHO cũng như các quy định chuyên môn hiện hành. Biên bản kiểm tra cần phải được phụ trách cơ sở cùng với trưởng đoàn kiểm tra ký xác nhận.
Bước 4: Nếu kết quả kiểm tra đáp ứng theo yêu cầu GMP thì cơ sở sẽ được cấp giấy chứng nhận, còn trong trường hợp cơ sở còn một số tồn tại có thể khắc phục được thì trong vòng 2 tháng kể từ ngày được kiểm tra, cơ sở phải khắc phục, sửa chữa và báo cáo kết quả khắc phục những tồn tại để gửi về Cục quản lý Dược. Đối với cơ sở chưa đáp ứng nguyên tắc, tiêu chuẩn GMP-WHO, cơ sở sản xuất sẽ cần tiến hành khắc phục, sửa chữa các tồn tại và nộp hồ sơ đăng ký như đăng ký kiểm tra lần đầu.
Bước 5: Cấp giấy chứng nhận cho cơ sở đăng ký
Hồ sơ xét Tiêu chuẩn GMP
- Bản đăng ký tái kiểm tra Thực hành tốt sản xuất thuốc (Mẫu số 02/GMP)
- Báo cáo những thay đổi của cơ sở trong 2 năm triển khai Thực hành tốt sản xuất thuốc
- Báo cáo hoạt động của cơ sở trong 2 năm qua
- Báo cáo khắc phục các tồn tại trong biên bản kiểm tra lần trước
- Báo cáo tóm tắt về huấn luyện, đào tạo của cơ sở trong 2 năm qua
- Báo cáo tự thanh tra và đánh giá của cơ sở trong đợt gần nhất (trong vòng 3 tháng) về triển khai Thực hành tốt sản xuất thuốc
Cùng với 4 tiêu chuẩn thực hành tốt GPs trong ngành Dược, GMP là tiêu chuẩn vô cùng quan trọng mà các cơ sở sản xuất thuốc, thực phẩm chức năng cần quan tâm. Sapo hy vọng rằng những chia sẻ trên của chúng tôi sẽ giúp bạn hiểu rõ về tiêu chuẩn GMP trong ngành Dược là gì để quản lý và tối ưu hoạt động sản xuất của các cơ sở một cách hiệu quả nhất.
Xem thêm: Chia sẻ kinh nghiệm và điều kiện mở quầy thuốc tây


